Стоматологи-терапевты Н. Тртич, Р. Арбутина, Ж. Кожич, В. Веселинович, (Босния и Герцеговина) и стоматолог-пародонтолог А. Босняк (Хорватия).
Balk J Dent Med 2016;Vol 20:149–154.
Агрессивный пародонтит представляет собой одну из самых тяжелых форм заболевания пародонта, приводящую к разрушению соединительного эпителия и альвеолярной кости вокруг зубов за очень короткий срок. Ранняя диагностика и своевременное лечение агрессивного пародонтита являются важнейшими факторами успеха сдерживания данного заболевания. Агрессивный пародонтит представляет собой одну из самых тяжелых форм заболевания пародонта, приводящую к разрушению соединительного эпителия и альвеолярной кости вокруг зубов за очень короткий срок. Ранняя диагностика и своевременное лечение агрессивного пародонтита являются важнейшими факторами успеха сдерживания данного заболевания.
Цель данного исследования заключалась в оценке эффективности двух различных методов обработки поддесневой области у пациентов с агрессивным пародонтитом.
Материалы и методы. В исследование было включено 46 пациентов обоих полов с диагностированным агрессивным пародонтитом. Пациентов разделили на две группы: исследуемую (PFLOW) и контрольную (снятие зубных отложений и сглаживание поверхности корня (SRP). Степень разрушения тканей пародонта определяли по уровню клинического прикрепления (CAL), уровень гигиены и воспаления десны оценивали с помощью общего индекса зубного налета (FMPS) и общего индекса кровоточивости (FMBS).
Результаты. Анализируемые показатели уменьшились в обеих группах.
Выводы. Воздушное полирование поддесневой области показала столь же хорошие результаты, как и SRP, но при этом обладала рядом преимуществ с точки зрения приемлемости для пациентов, временных затрат и безопасности для мягких тканей.
Ключевые слова: заболевание пародонта, агрессивный пародонтит, терапевтический подход, воздушная полировка поддесневой области.
ВВЕДЕНИЕ
Заболевания пародонта влекут за собой, помимо прочего, воспалительные и деструктивные изменения всего аппарата прикрепления зуба. Подобные изменения возникают как ответная реакция организма на присутствие бактерий в области зубодесневого соединения.1
Генерализованный агрессивный пародонтит является наиболее тяжелой, но не часто встречающейся формой данного заболевания. Его распространенность заметно варьируется в разных странах и зависит от этнической принадлежности пациента.2,3,4 К агрессивному пародонтиту может приводить множество причин, но, прежде всего, это неудовлетворительная гигиена полости рта, результатом которой становится аккумуляция бактерий, образующих биопленку.5,6 Еще одним важным фактором возникновения агрессивного пародонтита являются нарушения иммунной системы. Ряд авторов считает, что агрессивный пародонтит представляет собой результат снижения иммунной реакции организма на присутствие патогенов в биопленке. У пациентов с агрессивным пародонтитом наблюдается расстройство, затрагивающее функции нейтрофильных гранулоцитов и моноцитов.7
Поскольку этиология этого заболевания, судя по всему, многофакторна, его лечение весьма затруднено. Тем не менее, оно должно начинаться сразу же после выявления агрессивного пародонтита, равно как и других форм заболевания пародонта; результаты при этом чрезвычайно непредсказуемы.8
C учетом того, что у пациентов с агрессивным пародонтитом имеется генетическая предрасположенность к нему и наблюдаются нарушения иммунной системы, снижающие или даже полностью отключающие защиту тканей пародонта от бактерий, лечение агрессивного пародонтита подразумевает назначение антибиотиков, что придает этому заболеванию дополнительную специфичность.9,10,11
При этом основной терапевтической процедурой остается механическое удаление биопленки с наддесневых и поддесневых поверхностей. Пародонтальные карманы обрабатывают с помощью различных инструментов, конструкция которых позволяет относительно легко использовать их в наддесневой и поддесневой области. Технический прогресс позволил создать новые приспособления для обработки пораженного пародонта.12
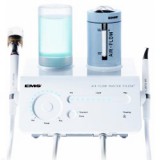
Новый, современный подход подразумевает воздушную полировку поверхностей корней с использованием мелкозернистых абразивных порошков. Эта процедура позволяет удалять с поверхности корней биопленку и другие мягкие отложения, а также цветовые изменения, за счет воздействия смеси сжатого воздуха, воды и глицинового порошка. Процедуру выполняют с помощью специального наконечника (рис. 1),13 повышающего эффективность смешивания воды, воздуха и порошка и одновременно с этим предотращающего эмфизему мягких тканей. Наконечник данной конструкции обеспечивает доступ в пародонтальные карманы глубиной до 5 мм. Воздушная полировка с помощью такого наконечника делает обработку поддесневой области более эффективной и комфортной для пациента.14

Рис. 1. Воздушная полировка поддесневой части зуба с помощью специального наконечника13
Агрессивный пародонтит представляет собой тяжелое заболевание пародонта: его своевременное выявление и принятие необходимых терапевтических мер являются важнейшими факторами, обуславливающими успех сдерживания пародонтита и предотвращения преждевременной утраты зубов. Цель данного исследования заключалась в определении клинической эффективности нового метода очищения пародонтальных карманов и в оценке степени разрушения тканей пародонта у курящих и некурящих пациентов.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование было включено 46 пациентов (28 женщин и 18 мужчин) в возрасте 25–47 лет (средний возраст 34,7 ± 6,5 лет) с диагностированным агрессивным пародонтитом. Участников исследования отбирали в соответствии с критериями диагностики агрессивного пародонтита, определенными Американской академией пародонтологии.15
В исследовании приняли участие как курящие, так и некурящие пациенты; среди последних были и те, кто никогда не курил, и отказавшиеся от курения, а в группу курильщиков входили пациенты, выкуривающие даже одну сигарету в день. Пациенты, включенные в исследование, не имели системных заболеваний в анамнезе и не принимали антибиотики в последние полгода.
Всех пациентов подробно информировали о предстоящих в рамках исследования процедурах; участие в исследовании приняли только те, кто дал на это добровольное письменное согласие.
В первое посещение пациентов попросили представить полную общемедицинскую/стоматологическую историю болезни, после чего они прошли клиническое обследование. Анализ рентгенограмм пациентов осуществляли в индивидуальном порядке. При оценке уровня гигиены полости рта и гингивита использовали следующие индексы: гигиену полости рта оценивали с помощью общего индекса зубного налета (FMPS), воспаление десен – с помощью общего индекса кровоточивости (FMBS).
Показатели FMPS и FMBS регистрировали в виде процентной доли поверхностей зубов с наддесневым налетом или кровоточивых участков в течение 15 с после зондирования зубодесневой борозды либо пародонтального кармана.16
Состояние пародонта оценивали, измеряя глубину пародонтальных карманов с помощью зонда (PP), а степень разрушения тканей пародонта определяли по уровню клинического прикрепления (CAL). Показатель CAL представляет собой расстояние между дном пародонтального кармана и цементно-эмалевой границей, выраженное в миллиметрах.17 Обследование пациентов проводили в стоматологическом кресле, при искусственном освещении и с помощью зеркала. Показатели измеряли с помощью пародонтологического зонда PCP-UNC 15 (Hu-Friedy). Параметры заносили в стандартную карту в соответствии с заранее определенной формулой. После обследования удалили имеющиеся у пациентов наддесневые отложения зубного камня, после чего участников исследования разделили на две группы.
В первой группе (SRP) биопленку из пародонтальных карманов удаляли с помощью скейлера Sonifl ex quick 2008 L (Kavo) и наконечников 5A 60°, 61° и 62°. Затем доступные поверхности корней полировали с помощью резиновых чашек.
Во второй группе (PFLOW) проводили поддесневую воздушную полировку корней. Воздушная полировка подразумевала направление струи сжатого воздуха, воды и глицинового пороша на поверхность корня с помощью специального наконечника AIR-FLOW MASTER (EMS). Каждую область обрабатывали в течение 4–5 с.
Курсовое лечение включало четыре посещения стоматолога. Пациенты осуществляли индивидуальную гигиену полости рта в соответствии с полученными от авторов инструкциями. Дважды в день, через 30 мин после чистки зубов, пациенты ополаскивали полость рта с помощью 0,12 % раствора биглюконата хлоргексидина (Curasept ADS 212, Curaden). По завершении курсового лечения пациентам назначили антибиотики, включая амоксициллин в капсулах по 500 мг и метронидазол в таблетках по 400 мг, три раза в день в течение 7 дней, в соответствии с рекомендациями Немецкого общества пародонтологии.18
Контрольные осмотры провели через 6 и 8 недель после первого посещения, причем во второй раз выполнили повторную оценку состояния тканей пародонта.
Второй этап исследования провели через 3 мес после начала лечения. Повторили все вышеописанные процедуры и измерения. Полученные результаты позволили принять решение о необходимости дальнейшего лечения.
СТАТИСТИЧЕСКИЙ АНАЛИЗ
Для сравнения наблюдений, сделанных до начала лечения и через 3 мес (в том случае, если они следовали нормальному распределению), использовали парный t-критерий Стьюдента. Статистически значимыми считались величины с P < 0,05. При проведении статистического анализа, а также составлении таблиц и диаграмм, использовали программы IBM SPSS Statistics 19.0, MS Office Word 2010 и MS Office Excel 2010.
РЕЗУЛЬТАТЫ
Индекс FMPS для группы PFLOW продемонстрировал статистически значимое снижение среднего показателя, с исходного уровня 44,28 до 15,86 через 3 мес лечения. Индекс FMPS для группы SRP также снизился статистически значимо, с 44,84 до 15,2 через 3 мес лечения (табл. 1).
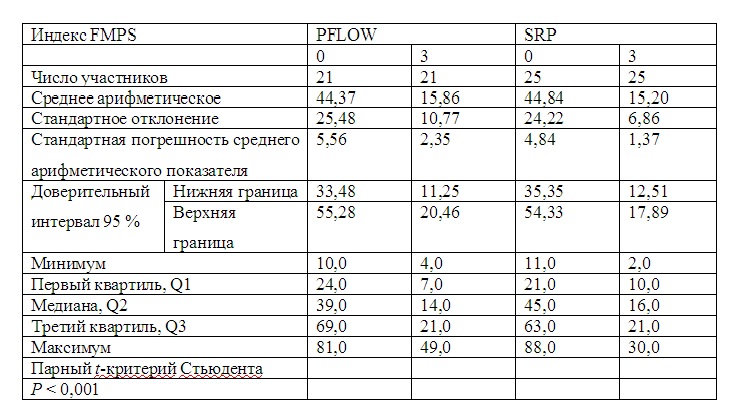
Таблица 1. Общий индекс зубного налета (FMPS) в зависимости от процедуры
Индекс FMBS для группы PFLOW продемонстрировал статистически значимое снижение среднего показателя, с исходного уровня 45,57 до 14,62 через 3 мес лечения. В случае группы SRP индекс FMBS также снизился статистически значимо, с 45,96 до 16,04 через 3 мес лечения (табл. 2).
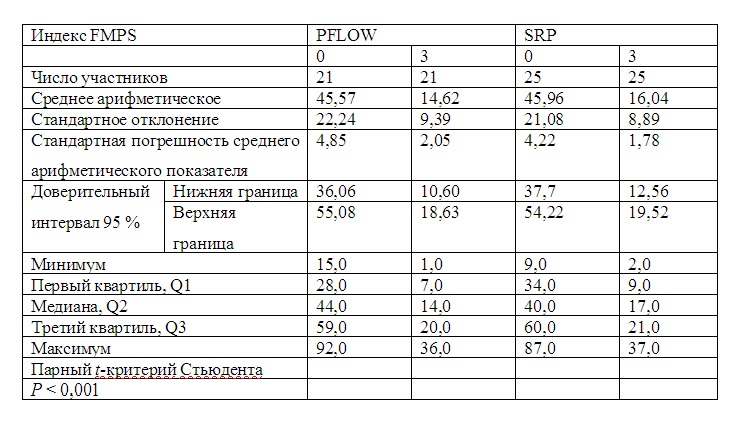
Таблица 2. Общий индекс кровоточивости (FMBS) в зависимости от процедуры
Индекс CAL для группы PFLOW продемонстрировал статистически значимое снижение среднего показателя, с исходного уровня 3,6 до 2,81 через 3 мес лечения. Индекс CAL для группы SRP также снизился статистически значимо, с 3,81 до 2,85 через 3 мес лечения (табл. 3).
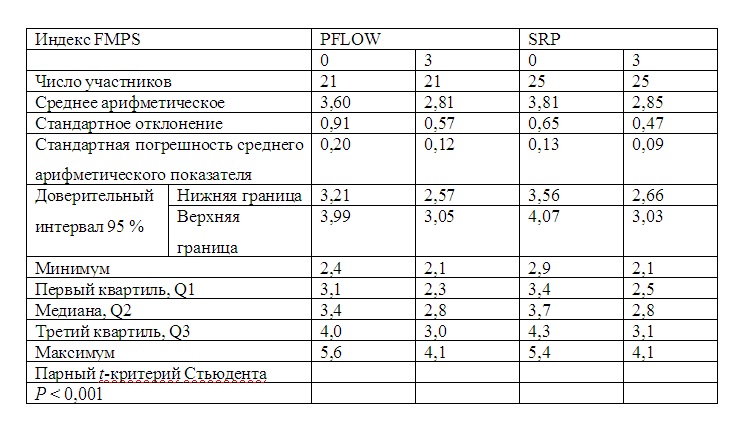
Таблица 3. Уровень клинического прикрепления (CAL) в зависимости от процедуры
Индекс CAL для группы некурящих пациентов продемонстрировал статистически значимое снижение среднего показателя, с исходного уровня 3,47 до 2,67 через 3 мес лечения. В случае курильщиков индекс CAL также снизился статистически значимо, с 4,01 до 3,02 через 3 мес лечения (табл. 4).
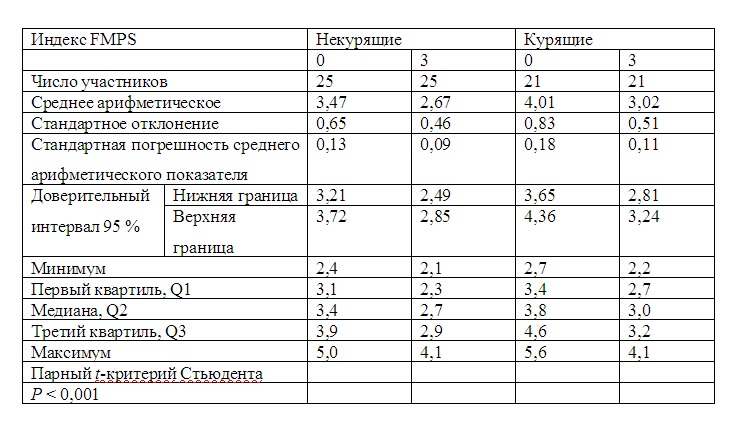
Таблица 4. Уровень клинического прикрепления (CAL) в зависимости от статуса
ОБСУЖДЕНИЕ
Заболевания пародонта широко распространены. Гингивит поражает существенную часть населения; более 90 % людей во всем мире в той или иной степени страдают воспалением десен.19 В целом осложненный пародонтит является шестым по частоте возникновения заболеванием в мире. Таким образом, этим заболеванием страдают 2 % молодых людей, а среди взрослых доля пациентов с осложненным пародонтитом составляет от 5 до 20 %.20 Данные по Боснии и Герцеговине (г. Баня-Лука и его окрестностям) неизвестны, поэтому данное исследование вносит определенный вклад и в изучение пародонтологического статуса местного населения.
Данное исследование было посвящено сравнению классической процедуры снятия зубных отложений и сглаживания поверхности корня с новым методом очищения пародонтальных карманов при помощи воздушной полировки. Для оценки состояния десен, уровня гигиены полости рта и воспаления десневых тканей использовались такие индексы, как FMPS и FMBS. Индекс CAL применялся для оценки степени разрушения тканей пародонта. Эффективность лечебных процедур была установлена путем мониторинга изменений этих индексов.
При сравнении индекса FMPS до и после лечения было отмечено его снижение в обеих группах, PFLOW и SRP. Сравнивая эти два метода Tomasi и соавт.21 получили сходные результаты: к концу лечения данный индекс значительно снизился.
Индекс FMBS применяется для оценки уровня гигиены полости рта. Обе группы, PFLOW и SRP, продемонстрировали статистически значимое снижение данного показателя по сравнению с исходными значениями. Показатели, полученные в рамках настоящего сравнения, согласуются с результатами других исследователей.16,22,23
Средний уровень клинического прикрепления (CAL) до начала обоих курсов лечения составил 3,71, что соответствует значительному разрушению тканей пародонта у пациентов с агрессивным пародонтитом. Усредненный исходный показатель CAL для группы PFLOW до начала лечения был равен 3,6, а через 3 мес лечения снизился до 2,81. Исходя из этого, можно заключить, что новый метод очищения пародонтальных карманов позволил остановить дальнейшее разрушение тканей пародонта.
В случае контрольной группы, участники которой подвергались звуковому снятию зубных отложений и сглаживанию поверхности корня, индекс CAL также снизился, что указывает на эффективный контроль заболевания пародонта. Другие исследования показали, что очищение пародонтальных карманов у пациентов с агрессивным пародонтитом вне зависимости от метода обработки ведет к предотвращению дальнейшего разрушения тканей пародонта.24
Согласно другим авторам, мониторинг параметров воспаления десен и индекса CAL показывает, что метод PFLOW можно считать альтернативой механическому звуковому снятию зубных отложений и сглаживанию поверхности корня, поскольку он позволяет эффективно удалять поддесневую биопленку, что ведет к предотвращению дальнейшего разрушения тканей пародонта.25
Доказано, что курение является значительным фактором риска развития агрессивного пародонтита.26 У курильщиков с первичными признаками пародонтита наблюдается более сильное разрушение альвеолярной кости и значительно более быстрая утрата клинического прикрепления, нежели у некурящих пациентов с агрессивным пародонтитом.27
Средний показатель CAL у некурящих участников исследования был равен 3,47, тогда как для курильщиков он составил 4,01, то есть, был на 0,54 выше. Это различие является статистически значимым и означает, что разрушение тканей пародонта при генерализованном агрессивном пародонтите в случае курильщиков выражено гораздо сильнее. Средний уровень клинического прикрепления через 3 мес лечения у некурящих пациентов составил 2,67, на 0,36 меньше, чем в случае курильщиков. Это различие также является статистически значимым и говорит о том, что вне зависимости от метода лечения у курящих пациентов с агрессивным пародонтитом сохраняется бóльшая выраженность разрушения тканей пародонта. В рамках настоящего исследования ткани пародонта некурящих пациентов, страдающих агрессивным пародонтитом, лучше реагировали на оба вида лечения.28 Другие исследователи, применявшие те же методы лечения, пришли к сходным выводам.29
Таким образом, результаты этого и других релевантных исследований говорят о том, что пациентов необходимо информировать о влиянии курения на пародонтологический статус. Курение ведет к гораздо более выраженному разрушению тканей пародонта. Стоматологи обязаны сообщать пациентам об этом факте и побуждать их немедленно отказаться от курения.
ВЫВОД
Хотя воздушное полирование поддесневой области и SRP продемонстрировали сопоставимые результаты, применение PFLOW обладает рядом преимуществ с точки зрения приемлемости для пациентов, временных затрат и безопасности для мягких тканей.
Разрушение тканей пародонта у курильщиков более выражено, нежели у некурящих пациентов, в то время как примененные в рамках данного исследования методы были одинаково эффективны в отношении как курильщиков, так и некурящих лиц.
Поскольку оба метода в сочетании с антибиотикотерапией приводили к существенному снижению клинических параметров заболевания, стоматолог должен выбирать способ лечения, исходя из его осуществимости и соответствия потребностям конкретного пациента.
Литература
- Pavlica D, Cakic S. Oralna mikrobiologija. Beograd: Zavod za udzbenike 2008.
- Albandar JM, Brown LJ, Löe H. Clinical features of ear ly-onset per iodont itis. J A Dent Assoc 1997;128:1393–1399.
- Harley AF, Floyd PD. Prevalence of juvenile periodontitis in schoolchildren in Lagos, Nigeria. Community Dent Oral Epidemiol 1988;16:299–301.
- Chan MC, Hyung KY, Seong NJ. Th e clinical assessment of aggressive periodontitis patients. J Periodontal Implant Sei 2011;41:143–148.
- Kobayashi T, Nagata T, Murakami S, Takashiba S, Kurihara H, Izumi Y. et al. Genetic risk factors for periodontitis in a Japanese population. J Dent Res 2009;88:1137–1141.
- de Carvalho FM, Tinoco EMB, Govil M, Marazita ML, Vieira AR. Aggressive periodontitis is likely infl uenced by a few small effect genes. J Clin Periodontol 2009;36:468–473.
- Tapashetti RP, Sharma S, Patil SR, Guwa S. Potential effect of neutrophil functional disorders on pathogenesis of aggressive periodontitis. J Contemp Dent Pract 2013;14:387–393.
- Noack B, Hoff mann T. Aggressive periodontitis. Perio 2004;1:335–344.
- Herrera D, Alonso B, Leon R, Roldän S, Sans M. Antimicrobial therapy in periodontitis :the use of systemic antimicrobials against the subgingival biofi lm. J Clin Periodont 2008;35:45–66.
- Kaner D, Chirstan C, Deitrich T, Bernimoulin JP, Kleber BM, Friedmann A. Timing affect the clinical outcome of adjunctive systemic antibiotic therapy for generalized aggressive periodontitis. J Periodontol 2007;78:1201–1208.
- Kulik EM, Lenkeit K, Chenaux S, Meyer J. Antimicrobial susceptibility of periodontopathogenic bacteria. J Antimicrob Chemothr 2008;61:1087–1091.
- Hodges K. Concepts in non-surgical periodontal therapy: Periodontal diagnosis and care planning. USA:Delmar, Th omson Learning; 1998.
- Subgingival air polishing. Available at: www.dentistryiq.com.
- Davis K. Biofilm removal with air polishing and subgingival air polishing. Available at: https://www.dentalacademyofce.com.
- American Academy of Periodontology Parametar on Aggressive Parodontitis. J Periodontol 2000;71:867–868.
- D’Ercole S, Piccolomini R, Capaldo G, Catamo G. Perinetti G. Guida L. Effectivness of ultrasonic instruments in the therapy of severe periodontitis: a comparative clinical-microbiological assessment with curettes. New Microbiologica 2006;29:101–110.
- Newman M.G, Takei H.H, Carranza F.A. Carranza’s clinical periodontology, 9th. Philadelphia: W.B. Saunders Co; 2002.
- Adjuvante Antibiotika in der Parodontitistherapie. Available at: http://www.dgzmk.de/uploads/tx_szdgzmkdocuments/Adjuvante_Antibiotika_in_der_Parodontitistherapie.pdf
- Coventry J, Griffi ths G, Scully C, Tonetti M. Periodontal disease. ABC of oral health. BMJ 2000;321:36–39.
- Marcenes W, Kassebaum NJ, Bernabe E, Flaxman A, Naghavi M, Lopez A, Murray CJ. Global burden of oral conditions in 1990-2010: a systematic analysis. J Dent Res 2013;92:592–597.
- Petersen PE, Bourgeois D, Ogawa H, Estupinan-Day S, Ndiaye C. Th e global burden of oral disease and risks to oral health. Bull World Health Organ 2005;83:661–669.
- Tomasi C, Bertelle A, Deilasega E, Wennström JL. Fullmouth ultrasonic debridement and risk of disease reccurrence: a 1-year follow-up. J Clin Periodontol 2006;33:626–631.
- Aimetti M, Romano F, Guzzi N. Carnevale G. Fullmouth disinfection and systemic antimicrobial therapy in generalized aggressive periodontitis. J Clin Periodontol 2012;39:284–294.
- Wennström JL, Dahlen G, Ramberg P. Subgingival debridement of periodontal pockets by air polishing in comparison with ultrasonic instrumentation during maintenance therapy. J Clin Periodontol 2011;38:820–827.
- Hägi TT, Hofmänner P, Salvi GE, Ramseier CA, Sculean A. Clinical outcomes following subgingival application of a novel erythritol powder by means of air polishing in supportive periodontal therapy: A randomized, controlled clinical study. Quintessence Int 2013;10:753–761.
- Haber J, Wattles J, Crowley M, Mandell R, Joshipura K, Kent RL. Evidence for cigarette smoking as a major risk factor for periodontitis. J Periodontol 1993;64:16–23.
- Genco RJ, Borgnakke WS. Risk factor for periodontal disease. Periodontol 2000 2013;62:59–94.
- Darby IB, Hodge PJ, Riggio MP, Kinane DF. Microbial comparison of smoker and non smoker adult and earlyonset periodontitis patients by polymerase chain reaction. J Clin Periodontol 2000;27:417–424.
- Kamma JJ, Nakou M, Baehni PC. Clinical and microbiological characteristics of smokers with early onset periodontitis. J Periodontal Res 1999;34:25–33.
Статья предоставлена компанией STI Dent (Россия) и опубликована с разрешения компании EMS (Швейцария).
► 31